- PRODUCTS產品介紹
- Cell Culture Cell Culture
- Animal Cell Culture Animal Cell Culture
- Insect Cell Culture Insect Cell Culture
- Stem Cell Culture Stem Cell Culture
- Immune Cell Culture Immune Cell Culture
- Antibiotic/Cytokine/Growth Factor Antibiotic/Cytokine/Growth Factor
- Cell Preparation Cell Preparation
- Cell Storage/Transportion Cell Storage/Transportion
- Cell Culture Supplements Cell Culture Supplements
- Cell Dissociation & Buffer Solutions Cell Dissociation & Buffer Solutions
- Extracellular Matrix Extracellular Matrix
- Cell Isolation Cell Isolation
- Human Platelet Lysate Human Platelet Lysate
- Animal Cell Culture
- Cell Therapy Cell Therapy
- MSC
- NK
- CIK
- T Cell
- DC
- iPS
- Stem Cell-CD34 Stem Cell-CD34
- Adipose Stem Cell Adipose Stem Cell
- Water-Free Thawing System Water-Free Thawing System
- Blood biopsy preparation Blood biopsy preparation
- Quality Control Quality Control
- GMP Grade Cytokine GMP Grade Cytokine
- Common Chemicals & Buffers & Lab Tools Common Chemicals & Buffers & Lab Tools
- Life Science Life Science
- Exosome Research Exosome Research
- Spectradyne-Microfluidic Nanoparticle Analysis
- Corning-VideoDrop
- Immunostep- Lyophilized Exosome Standards
- Immunostep-ExoStep Platform
- Immunostep-Exosome Isolation Columns (SEC)
- GeneCopoeia Lentifect™ Exosome Labeling Lentiviral
- GeneCopoeia miProfile™ Exosome miRNA qPCR arrays
- Exosome Memebrane / Protein Dye
- DNA/RNA Research
- miRNA/shRNA/siRNA Research
- Protein Research
- In Vivo Assay In Vivo Assay
- Cloning & Clone Collection
- Transfection & Transduction
- IHC
- Cell-Based Assay
- Mitochondria Research Mitochondria Research
- Antibody/Antigen
- ELISA ELISA
- Antibody Labeling Antibody Labeling
- mRNA/Oligos/Nucleotide
- Microbial Research Microbial Research
- Ultra high content imaging
- Tumor Research Tumor Research
- Microarray Microarray
- Exosome Research
- Pharma Manufacturing & QC Pharma Manufacturing & QC
- Impurity Detection
- Micoplasma Detection Micoplasma Detection
- Endotoxin Remove Endotoxin Remove
- Visual Inspection Visual Inspection
- Mycobacteria Detection Mycobacteria Detection
- Nanoparticle Analyzer Nanoparticle Analyzer
- Cell Culture
- NEWS最新消息
- PROMOTIONS促銷活動
- SUPPLIER代理品牌
- AAjinomoto-iPSAbcamAbebioAbbexaAbcoreAlpha-TecAkadeum
- BBiCell ScientificBIO-HELIXBiolineBioLife SolutionsBio X Cell
- CCorningCYGNUSCompass BiomedicalCUSABIOCytori Therapeutics IncCANDOR BioscienceCreative BioMart
- DDojindo
- EExpression SystemsEastCoast BioElixirgen Scientific
- FFast Forward DiscoveriesFortius BioFisher Scientific
- GGoldBioGenlantisGeneCopoeia
- HHyTest Ltd
- IImmunostepiRealIrvine ScientificInVitriaImmuno-Biological Laboratories
- KKohjin BioKingfisher Biotech
- LLIPOSOMA ─ Clodronate Liposomes
- MMatrixome & NippiMedicagoMeridian Life Science
- NNonacus
- QQIAGEN
- PProtein ArkProFoldin-ProteomicsProSpec
- SSHIMADZUSignaGenScyTek Laboratories IncSMOBIOSpectradyne
- TTriLink BiotechnologiesTymora Analytical
- WWorthingtonWaken X BioLife Solutions
- ABOUT關於我們
- CONTACT聯絡我們
- 產品介紹
- Cell Culture Cell Culture
- Animal Cell Culture Animal Cell Culture
- Insect Cell Culture Insect Cell Culture
- Stem Cell Culture Stem Cell Culture
- Immune Cell Culture Immune Cell Culture
- Antibiotic/Cytokine/Growth Factor Antibiotic/Cytokine/Growth Factor
- Cell Preparation Cell Preparation
- Cell Storage/Transportion Cell Storage/Transportion
- Cell Culture Supplements Cell Culture Supplements
- Cell Dissociation & Buffer Solutions Cell Dissociation & Buffer Solutions
- Extracellular Matrix Extracellular Matrix
- Cell Isolation Cell Isolation
- Human Platelet Lysate Human Platelet Lysate
- Animal Cell Culture
- Cell Therapy Cell Therapy
- MSC
- NK
- CIK
- T Cell
- DC
- iPS
- Stem Cell-CD34 Stem Cell-CD34
- Adipose Stem Cell Adipose Stem Cell
- Water-Free Thawing System Water-Free Thawing System
- Blood biopsy preparation Blood biopsy preparation
- Quality Control Quality Control
- GMP Grade Cytokine GMP Grade Cytokine
- Common Chemicals & Buffers & Lab Tools Common Chemicals & Buffers & Lab Tools
- Life Science Life Science
- Exosome Research Exosome Research
- Spectradyne-Microfluidic Nanoparticle Analysis
- Corning-VideoDrop
- Immunostep- Lyophilized Exosome Standards
- Immunostep-ExoStep Platform
- Immunostep-Exosome Isolation Columns (SEC)
- GeneCopoeia Lentifect™ Exosome Labeling Lentiviral
- GeneCopoeia miProfile™ Exosome miRNA qPCR arrays
- Exosome Memebrane / Protein Dye
- DNA/RNA Research
- miRNA/shRNA/siRNA Research
- Protein Research
- In Vivo Assay In Vivo Assay
- Cloning & Clone Collection
- Transfection & Transduction
- IHC
- Cell-Based Assay
- Mitochondria Research Mitochondria Research
- Antibody/Antigen
- ELISA ELISA
- Antibody Labeling Antibody Labeling
- mRNA/Oligos/Nucleotide
- Microbial Research Microbial Research
- Ultra high content imaging
- Tumor Research Tumor Research
- Microarray Microarray
- Exosome Research
- Pharma Manufacturing & QC Pharma Manufacturing & QC
- Impurity Detection
- Micoplasma Detection Micoplasma Detection
- Endotoxin Remove Endotoxin Remove
- Visual Inspection Visual Inspection
- Mycobacteria Detection Mycobacteria Detection
- Nanoparticle Analyzer Nanoparticle Analyzer
- Cell Culture
- 最新消息
- 促銷活動
- 代理品牌
- AAjinomoto-iPSAbcamAbebioAbbexaAbcoreAlpha-TecAkadeum
- BBiCell ScientificBIO-HELIXBiolineBioLife SolutionsBio X Cell
- CCorningCYGNUSCompass BiomedicalCUSABIOCytori Therapeutics IncCANDOR BioscienceCreative BioMart
- DDojindo
- EExpression SystemsEastCoast BioElixirgen Scientific
- FFast Forward DiscoveriesFortius BioFisher Scientific
- GGoldBioGenlantisGeneCopoeia
- HHyTest Ltd
- IImmunostepiRealIrvine ScientificInVitriaImmuno-Biological Laboratories
- KKohjin BioKingfisher Biotech
- LLIPOSOMA ─ Clodronate Liposomes
- MMatrixome & NippiMedicagoMeridian Life Science
- NNonacus
- QQIAGEN
- PProtein ArkProFoldin-ProteomicsProSpec
- SSHIMADZUSignaGenScyTek Laboratories IncSMOBIOSpectradyne
- TTriLink BiotechnologiesTymora Analytical
- WWorthingtonWaken X BioLife Solutions
- 關於我們
- 聯絡我們
News
HomeNews
2024/03/01
TriLink|研究聚焦:體內 Prime Editing ── 透過脂質奈米顆粒 (LNP) 完成傳遞

藉由 Prime editing(PE)能精準地改寫基因組中的遺傳訊息,此技術具有徹底改變治療發展史的巨大潛力。然而,PE 的臨床應用由於缺乏有效的體內遞送方法而受到阻礙。近年來,脂質奈米顆粒(LNP)作為病毒載體遞送核酸分子的替代品而受到廣泛關注。

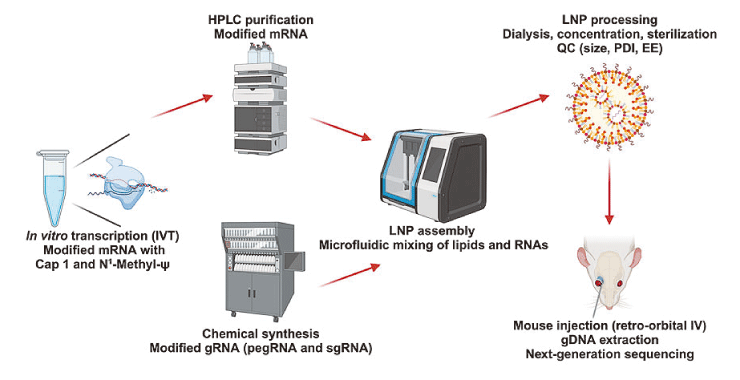
本篇文獻為最初使用 LNP 作為遞送系統的體內 PE 的文章。馬薩諸塞大學醫學院(UMass Chan)的研究人員證明,將化學修飾的 prime editing guide RNA(pegRNA)和 prime editor messenger RNA(PE mRNA)一同送入野生型小鼠中能夠在其身上進行所需的編輯,並且藉由 LNP 的傳送可使 PE 在免疫缺陷小鼠上作用的效率增加。本研究使用 TriLink 的專利 CleanCap® Reagent AG (3' OMe) 和 N1-Methylpseudouridine-5'-Triphosphate。
化學修飾的 pegRNA 和 PE mRNA 可於體外進行高效率的 Prime Editing
馬薩諸塞大學研究人員利用兩種 PE 對小鼠 Pcsk9 基因進行編輯:+3-5 GCG 到 TTA 替換或插入 +1 TTAC。以電穿孔方式將 pegRNA 與 PE mRNA(以 CleanCap AG 3'OMe analog 並含有 N1-methyl-pseudouridine 修飾)送進小鼠 Hepa1-6 細胞,接著以次世代定序(NGS)定量正確編輯和插入缺失的百分比。其中以插入+1 TTAC 的方式在生成所需編輯表現出更高的效率,因此選擇此方式用於未來的研究。作者最初設計了一系列具有不同修飾模式的 pegRNA,以篩選出能在體外維持高效率 PE 的 pegRNA。
LNP 傳遞化學修飾的 pegRNA 和 PE mRNA 進行體內 Prime Editing
接下來,馬薩諸塞大學研究人員藉由以 LNP 傳遞的方式研究基因編輯器在體內的表現情形。他們將 Pcsk9 single-guide RNA (sgRNA) 與 SpyCas9 mRNA 共同包裝在 LNP 中並送至小鼠中以探討肝臟組織中的基因編輯的狀況。基因編輯結果證實 LNP 的效果,LNP 接著也被用於共同遞送化學修飾的 pegRNA 與 PE mRNA 進行 prime editing,其結果與體外研究結果一致。
透過適當的重新給藥來增強體內 Prime Editing
為了驗證重新給藥是否能提高體內 PE 效率,馬薩諸塞大學研究人員將單次 60 µg 劑量與每日 5 次 60 µg 劑量進行了比較,並以 NGS 來測量肝臟中的 prime editing 效率。然而,每日給藥並沒有提高 PE 效率,反而引起嚴重的肝毒性和異常。研究人員改用以頻率較低的給藥方案(每週 60 µg,持續三週)克服了這些副作用,也將 PE 效率提高了 1.8 倍。
在免疫缺陷小鼠模型中能使 PE 效率提高
作者假設在每日重複給藥實驗中,編輯效率並無增強的原因是由於先天免疫反應,其限制了 RNA 的轉譯作用。為了探索此假設,馬薩諸塞大學的研究人員將一組免疫缺陷小鼠(NOD scid gamma,或 NSG)納入每週重複給藥實驗中。 結果顯示,NSG 小鼠單劑量(3 mg/kg)的 PE 效率是野生型小鼠的 2.8 倍,此發現需要進一步研究以確定是否與免疫相關。
未來展望
LNP 作為體內 prime editing 的遞送系統的成功,代表了基因工程醫學領域的重大發展。為了其進一步的進展,研究人員需要考慮的因素包括 RNA 設計、給藥方案和 LNP 組成等,並探討免疫相關因素的重要性。
原始文章>>
TriLink 特色產品
參考文獻:Article reference: Chen, Z., Kelly, K., Cheng, H. et al. In Vivo Prime Editing by Lipid Nanoparticle Co-Delivery of Chemically Modified pegRNA and Prime Editor mRNA. GEN Biotechnology 2(6):490-502 (2023).
