- PRODUCTS產品介紹
- Cell Culture Cell Culture
- Animal Cell Culture Animal Cell Culture
- Insect Cell Culture Insect Cell Culture
- Stem Cell Culture Stem Cell Culture
- Immune Cell Culture Immune Cell Culture
- Antibiotic/Cytokine/Growth Factor Antibiotic/Cytokine/Growth Factor
- Cell Preparation Cell Preparation
- Cell Storage/Transportion Cell Storage/Transportion
- Cell Culture Supplements Cell Culture Supplements
- Cell Dissociation & Buffer Solutions Cell Dissociation & Buffer Solutions
- Extracellular Matrix Extracellular Matrix
- Cell Isolation Cell Isolation
- Human Platelet Lysate Human Platelet Lysate
- Animal Cell Culture
- Cell Therapy Cell Therapy
- MSC
- NK
- CIK
- T Cell
- DC
- iPS
- Stem Cell-CD34 Stem Cell-CD34
- Adipose Stem Cell Adipose Stem Cell
- Water-Free Thawing System Water-Free Thawing System
- Blood biopsy preparation Blood biopsy preparation
- Quality Control Quality Control
- GMP Grade Cytokine GMP Grade Cytokine
- Common Chemicals & Buffers & Lab Tools Common Chemicals & Buffers & Lab Tools
- Life Science Life Science
- Exosome Research Exosome Research
- Spectradyne-Microfluidic Nanoparticle Analysis
- Corning-VideoDrop
- Immunostep- Lyophilized Exosome Standards
- Immunostep-ExoStep Platform
- Immunostep-Exosome Isolation Columns (SEC)
- GeneCopoeia Lentifect™ Exosome Labeling Lentiviral
- GeneCopoeia miProfile™ Exosome miRNA qPCR arrays
- Exosome Memebrane / Protein Dye
- DNA/RNA Research
- miRNA/shRNA/siRNA Research
- Protein Research
- In Vivo Assay In Vivo Assay
- Cloning & Clone Collection
- Transfection & Transduction
- IHC
- Cell-Based Assay
- Mitochondria Research Mitochondria Research
- Antibody/Antigen
- ELISA ELISA
- Antibody Labeling Antibody Labeling
- mRNA/Oligos/Nucleotide
- Microbial Research Microbial Research
- Ultra high content imaging
- Tumor Research Tumor Research
- Microarray Microarray
- Exosome Research
- Pharma Manufacturing & QC Pharma Manufacturing & QC
- Impurity Detection
- Micoplasma Detection Micoplasma Detection
- Endotoxin Remove Endotoxin Remove
- Visual Inspection Visual Inspection
- Mycobacteria Detection Mycobacteria Detection
- Nanoparticle Analyzer Nanoparticle Analyzer
- Cell Culture
- NEWS最新消息
- PROMOTIONS促銷活動
- SUPPLIER代理品牌
- AAjinomoto-iPSAbcamAbebioAbbexaAbcoreAlpha-TecAkadeum
- BBiCell ScientificBIO-HELIXBiolineBioLife SolutionsBio X Cell
- CCorningCYGNUSCompass BiomedicalCUSABIOCytori Therapeutics IncCANDOR BioscienceCreative BioMart
- DDojindo
- EExpression SystemsEastCoast BioElixirgen Scientific
- FFast Forward DiscoveriesFortius BioFisher Scientific
- GGoldBioGenlantisGeneCopoeia
- HHyTest Ltd
- IImmunostepiRealIrvine ScientificInVitriaImmuno-Biological Laboratories
- KKohjin BioKingfisher Biotech
- LList LabsLIPOSOMA ─ Clodronate Liposomes
- MMatrixome & NippiMedicagoMeridian Life Science
- NNonacus
- QQIAGEN
- PProtein ArkProFoldin-ProteomicsProSpec
- SSHIMADZUSignaGenScyTek Laboratories IncSMOBIOSpectradyne
- TTriLink BiotechnologiesTymora Analytical
- WWorthingtonWaken X BioLife Solutions
- ABOUT關於我們
- CONTACT聯絡我們
- 產品介紹
- Cell Culture Cell Culture
- Animal Cell Culture Animal Cell Culture
- Insect Cell Culture Insect Cell Culture
- Stem Cell Culture Stem Cell Culture
- Immune Cell Culture Immune Cell Culture
- Antibiotic/Cytokine/Growth Factor Antibiotic/Cytokine/Growth Factor
- Cell Preparation Cell Preparation
- Cell Storage/Transportion Cell Storage/Transportion
- Cell Culture Supplements Cell Culture Supplements
- Cell Dissociation & Buffer Solutions Cell Dissociation & Buffer Solutions
- Extracellular Matrix Extracellular Matrix
- Cell Isolation Cell Isolation
- Human Platelet Lysate Human Platelet Lysate
- Animal Cell Culture
- Cell Therapy Cell Therapy
- MSC
- NK
- CIK
- T Cell
- DC
- iPS
- Stem Cell-CD34 Stem Cell-CD34
- Adipose Stem Cell Adipose Stem Cell
- Water-Free Thawing System Water-Free Thawing System
- Blood biopsy preparation Blood biopsy preparation
- Quality Control Quality Control
- GMP Grade Cytokine GMP Grade Cytokine
- Common Chemicals & Buffers & Lab Tools Common Chemicals & Buffers & Lab Tools
- Life Science Life Science
- Exosome Research Exosome Research
- Spectradyne-Microfluidic Nanoparticle Analysis
- Corning-VideoDrop
- Immunostep- Lyophilized Exosome Standards
- Immunostep-ExoStep Platform
- Immunostep-Exosome Isolation Columns (SEC)
- GeneCopoeia Lentifect™ Exosome Labeling Lentiviral
- GeneCopoeia miProfile™ Exosome miRNA qPCR arrays
- Exosome Memebrane / Protein Dye
- DNA/RNA Research
- miRNA/shRNA/siRNA Research
- Protein Research
- In Vivo Assay In Vivo Assay
- Cloning & Clone Collection
- Transfection & Transduction
- IHC
- Cell-Based Assay
- Mitochondria Research Mitochondria Research
- Antibody/Antigen
- ELISA ELISA
- Antibody Labeling Antibody Labeling
- mRNA/Oligos/Nucleotide
- Microbial Research Microbial Research
- Ultra high content imaging
- Tumor Research Tumor Research
- Microarray Microarray
- Exosome Research
- Pharma Manufacturing & QC Pharma Manufacturing & QC
- Impurity Detection
- Micoplasma Detection Micoplasma Detection
- Endotoxin Remove Endotoxin Remove
- Visual Inspection Visual Inspection
- Mycobacteria Detection Mycobacteria Detection
- Nanoparticle Analyzer Nanoparticle Analyzer
- Cell Culture
- 最新消息
- 促銷活動
- 代理品牌
- AAjinomoto-iPSAbcamAbebioAbbexaAbcoreAlpha-TecAkadeum
- BBiCell ScientificBIO-HELIXBiolineBioLife SolutionsBio X Cell
- CCorningCYGNUSCompass BiomedicalCUSABIOCytori Therapeutics IncCANDOR BioscienceCreative BioMart
- DDojindo
- EExpression SystemsEastCoast BioElixirgen Scientific
- FFast Forward DiscoveriesFortius BioFisher Scientific
- GGoldBioGenlantisGeneCopoeia
- HHyTest Ltd
- IImmunostepiRealIrvine ScientificInVitriaImmuno-Biological Laboratories
- KKohjin BioKingfisher Biotech
- LList LabsLIPOSOMA ─ Clodronate Liposomes
- MMatrixome & NippiMedicagoMeridian Life Science
- NNonacus
- QQIAGEN
- PProtein ArkProFoldin-ProteomicsProSpec
- SSHIMADZUSignaGenScyTek Laboratories IncSMOBIOSpectradyne
- TTriLink BiotechnologiesTymora Analytical
- WWorthingtonWaken X BioLife Solutions
- 關於我們
- 聯絡我們
News
HomeNews
2018/01/08
【BioLife Solutions】全球首個關節炎細胞和基因療法-Invossa在韓國上市!
 |
 |
||||||||||||||||||||||||||||||||||||||
| 全球首個關節炎細胞和基因療法產品在韓國上市! | |||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||
| Kolon Life Science已開始在南韓銷售骨關節炎藥Invossa 註1 | 單次注射此藥物,可緩解疼痛病症長達兩年時間。此療法用於即使接受止痛藥或物理治療三個月以上仍然會出現疼痛的膝關節骨性關節炎患者,未來Inovossa將幫助各地診所和大醫院在內的膝關節骨關節炎患者。目前還沒有退化性骨關節炎的治療方法,Inovossa藥物僅被批准用於退化性關節炎的疼痛緩解和功能改善,限制了其治療應用。TissueGene正進行臨床試驗證明該藥物可以幫助組織再生。 BioLife Solutions近年來不斷的致力於幫助再生醫學與細胞治療產業的進步,提供優化的細胞凍存液。此一新聞能使廣大的客戶更安心地在細胞和基因療法的產品製造過程中使用CryoStor細胞凍存液。 |
||||||||||||||||||||||||||||||||||||||
| 第一名患者首次在2017年11月8日接受注射,韓國食品和藥物安全部於2017年7月批准了Invossa的上市 註2。Invossa是一種治療退化性關節炎的新型細胞介導療法(cell-mediated therapy),更是世界上第一個治療膝關節骨性關節炎的細胞和基因療法。此種關節疾病起因為關節軟骨退化磨損,導致骨頭摩擦引起疼痛。 Invossa是由Kolon集團在美國的子公司TissueGene開發的,已在KOSDAQ上市,由首爾KolonLife Science負責Invossa在韓國的營銷和銷售。早在2016年12月BioLife Solutions與Tissue Gene公司簽署了10年供應合約,使用cGMP等級凍存液於Invossa細胞和基因療法產品製造過程中。Invossa產品被凍存於BioLife Solutions的CryoStor細胞凍存液中被運送,以延長保存期限,直到送達診所後注射入病人體內。 註1:新聞出處 註2:新聞出處 |
|||||||||||||||||||||||||||||||||||||||
| CryoStor® CS2, CS5 & CS10細胞凍存液 cGMP Grade Biopreservation Media for Cells and Tissues |
|||||||||||||||||||||||||||||||||||||||
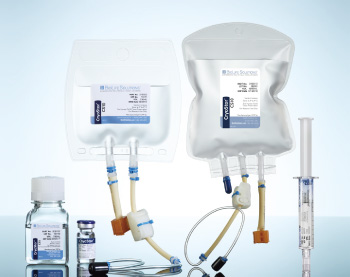 |
● 無血清成分 ● 無蛋白質成分 ● 無動物來源成分 ● 已申請通過美國FDA DMF |
||||||||||||||||||||||||||||||||||||||
| CryoStor®系列產品為預先配製、最優化的細胞凍存液,專為在超低溫度的環境下 (-80 到 -196ºC) 保存細胞所設計。CryoStor®內含不同濃度的USP等級DMSO,於冷凍保存的過程中透過調節分子生物反應、減少細胞內冰晶形成,為細胞在凍結、存儲和解凍過程中提供一個安全與保護的環境。CryoStor®的特殊配方讓細胞在不含血清、蛋白質和其餘高含量細胞毒性藥物下增強活力和功能,減少保存後細胞壞死和凋亡。所有原料皆為美國藥典 (USP) 等級,在符合cGMP規範下製造生產。為無血清、無蛋白質、無動物來源成分的細胞凍存液。 | |||||||||||||||||||||||||||||||||||||||
| CryoStor®預先用DMSO以2%、5%和10%的濃度配製,提供以下幾種包裝: | |||||||||||||||||||||||||||||||||||||||
| Ordering Information | |||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||
